基礎(chǔ)×臨床《Nano Today》:溫醫(yī)大眼視光沈建良課題組聯(lián)合臨床團隊創(chuàng)新構(gòu)建多功能納米治療系統(tǒng),助力細菌性角膜炎協(xié)同治療

細菌性角膜炎(Bacterial Keratitis, BK)是全球視力損害及致盲的重要病因,其傳統(tǒng)治療手段——局部高頻次抗生素滴注不僅易誘導(dǎo)細菌耐藥性,且因藥物在眼表滯留時間短、角膜滲透性差導(dǎo)致生物利用度低,同時未能有效解決感染后角膜基質(zhì)瘢痕增生這一關(guān)鍵臨床問題,存在顯著的局限性。
針對該臨床難題,溫州醫(yī)科大學(xué)附屬眼視光醫(yī)院沈建良研究員課題組和角膜與眼表疾病中心臨床團隊展開聯(lián)合攻關(guān),通過創(chuàng)新性構(gòu)建多功能納米治療系統(tǒng)DHA-lys@miRNA,成功實現(xiàn)了針對細菌性角膜炎的抗感染與抗纖維化的協(xié)同治療。近日,相關(guān)成果以“A multistage microRNA nanotherapeutic to address fibrosis of bacterial keratitis - ScienceDirect”為題于Nano Today期刊(中科院1區(qū)TOP,IF=13.2)在線發(fā)表。
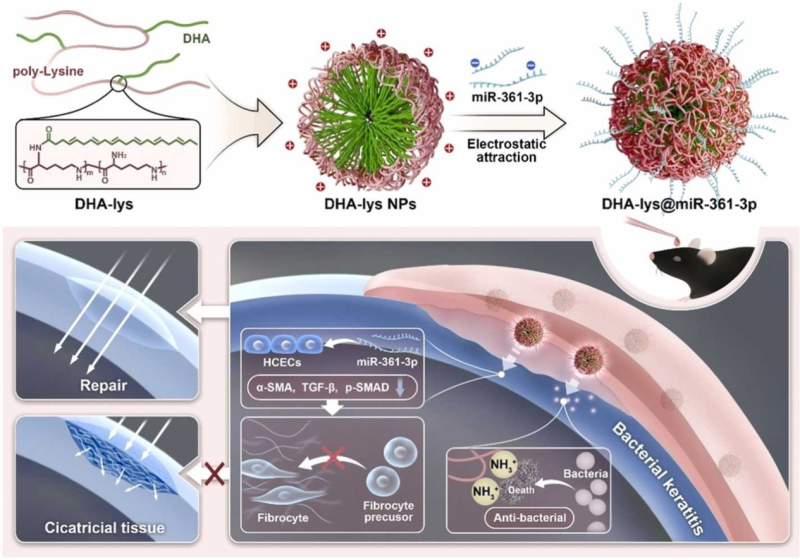
研究團隊基于構(gòu)建的兩親性陽離子納米載體DHA-lys,并通過靜電相互作用負載治療性microRNA形成復(fù)合納米體系。該體系展現(xiàn)出以下突出優(yōu)勢:
(1)載體材料本身具有顯著的廣譜抗菌活性,其陽離子特性可破壞細菌細胞膜完整性;
(2)獨特的雙親分子結(jié)構(gòu)使納米顆粒能夠同時與淚膜脂質(zhì)層和黏蛋白層形成多重相互作用,角膜滯留時間、藥物滲透效率較傳統(tǒng)制劑均有顯著改善;
(3)通過生物信息學(xué)篩選聯(lián)合體內(nèi)外實驗驗證,首次揭示miR-361–3p可通過調(diào)控角膜基質(zhì)細胞-肌成纖維細胞轉(zhuǎn)化(CMT-Myofibroblast Transition)通路,特異性抑制TGF-β/Smad信號傳導(dǎo),使角膜瘢痕面積減少。
在BK小鼠模型中,DHA-lys@miRNA納米治療組展現(xiàn)出顯著的協(xié)同療效,同時角膜透明度評分也得到改善。組織病理學(xué)分析證實,該體系可有效維持角膜基質(zhì)膠原纖維的正常排列,抑制病理性ECM沉積。
這種"抗菌-抗纖維化"雙功能整合策略突破了傳統(tǒng)單一療法的局限,為感染性眼病的精準治療提供了新范式。本研究不僅拓展了核酸納米藥物在眼科的應(yīng)用邊界,更為開發(fā)多靶點協(xié)同治療系統(tǒng)奠定了重要理論基礎(chǔ)。
近年來,溫醫(yī)大眼視光醫(yī)院積極踐行"臨床問題驅(qū)動應(yīng)用基礎(chǔ)研究,科研成果反哺臨床實踐"的發(fā)展理念,大力推動學(xué)科交叉合作、基礎(chǔ)-臨床深度融合,科技創(chuàng)新活力持續(xù)澎湃。本次沈建良研究員課題組與角膜病臨床團隊的深度合作,正是醫(yī)院構(gòu)建"臨床-基礎(chǔ)"雙向賦能通道的典范成果。未來,醫(yī)院將持續(xù)優(yōu)化多學(xué)科交叉創(chuàng)新機制,進一步發(fā)揮基礎(chǔ)、臨床團隊協(xié)同攻關(guān)優(yōu)勢,破解更多醫(yī)學(xué)難題,為眼病患者的健康保駕護航。

友情鏈接

官方微博

微信公眾平臺